İMMÜN ARACILI DOKU HASARININ MEKANİZMALARI VE HİPERSENSİTİVİTE REAKSİYONLARI
Kazanılmış immün yanıt; infeksiyonlara karşı konak savunmasının önemli bir parçasıdır. Antijenlere spesifik reseptör taşıyan lenfositlerin klonal seleksiyonu sayesinde bu savunmanın özgül ayırıcı ve benzersiz yanı ise patojenleri spesifik olarak tanıyabilme yeteneğidir. İnfeksiyöz ajanlarla ilgisiz bazı antijenler de kazanılmış immün yanıt ile karşılanırlar. Klinik olarak önemli birçok hastalık, tipik olarak infeksiyonun olmadığı durumlarda bazı antijenlere karşı oluşmuş normal immün yanıtla karakterizedir. Örneğin alerjik hastalıklardaki immünolojik yanıt, infeksiyöz olmayan ajanlara karşıdır. Aslında bu olaydaki antijen zararsız bir çevre elemanıdır. Otoimmünitede ise immün yanıt otoantijene yöneliktir.
Kazanılmış immün yanıtta patojenleri elimine eden efektör mekanizmalar, doğuştan var olan immün mekanizmalara benzerdir. Aradaki en önemli farklardan biri; kazanılmış yanıtın spesifik antijen tanıyabilme özelliğidir. Doğuştan var olan immün mekanizmalarda ise bu özellik yoktur; her türlü antijenik uyarıya benzer cevap verilir. Ancak, kazanılmış immün sitemin efektör hücreleri olan B ve T lenfositlerinin görevlerini yapabilmeleri için inflamatuvar hücreler ve doğuştan var olan immün sistem molekülleri gereklidir.
Kazanılmış İmmün Sistemin Efektör Mekanizmaları
Antikorların efektör etkileri hemen hemen daima inisiyal immün sistem moleküllerinin ve hücrelerinin aktive edilmesine bağlıdır. Antikorlar, antijenlerin spesifik olmayan inflamatuvar hücrelere bağlanmasını sağlayan adaptör moleküllerdir ve bu iflamatuvar hücrelerin yıkıcı efektör yanıtlarını kontrol ederler. Antikorlar ayrıca antijenlerin opsonizasyonunu arttıran, fagositleri çağıran ve antikor aracılı hasarı güçlendiren kompleman sistemini de aktive ederek görev yaparlar. Üretilen antikorların izotipi veya sınıfı hangi tip efektör mekanizmanın çalışacağını belirler.
İmmünglobülinler için oluşmuş reseptörler, immün kaskadın humoral ve hücresel fazları arasında bağlantı kurarlar; bunlar aynı zamanda yabancı ve endojen materyalin opsonize edilerek tanınması ve yok edilmesi işleminde de önemli bir role sahiptirler. Bazı hücrelerde antikorlar için var olan bağlanma yerleri Fc reseptörler olarak adlandırılır ve antijen spesifitesinden bağımsız olarak belli bir antikorun immünglobülinin ağır zincirinin Fc kısmıyla ilişki kurarlar. Herhangi bir spesifitesi olmayan immünolojik hücreler (nötrofil, makrofaj, mast hücreleri gibi), Fc reseptörlerinin antijen spesifik antikorlarla etkileşmesi sonucu, inflamatuvar yanıtta yer almak üzere var olurlar. Farklı efektör hücrelerde, farklı immünoglobülin izotipleri için farklı reseptörler eksprese edilir.
IgG için reseptörler; hematopoetik hücre yüzey molekülü olarak fagositlerin (makrofajlar, monositler, nötrofiller), trombositlerin, mast hücrelerinin, eozinofillerin ve doğal katil hücrelerin yüzeyinde eksprese edilen çeşitli reseptörlerdir. Fcγ reseptörler olarak adlandırılırlar ve bu reseptörler genellikle hem stimulatör hem de inhibitör etkili çiftler olarak ekprese edilirler. Stimulasyonu tetikleyen Fcγ reseptörleri fagositozu, antikor bağımlı hücre aracılıklı sitotoksisiteyi, granüllerin sekresyonunu ve inflamatuvar medyatörlerin (proteazlar, sitokinler, reaktif oksidanlar gibi) salınımını başlatır. Fcγ reseptörleri ailesinin üyeleri arasındaki geniş yapısal çeşitlilik; bağlanma kapasitesinde, sinyal iletiminde, hücre tipi spesifik ekspresyon patterninde farklılıklara öncülük eder. Bu çeşitlilik IgG komplekslerinin inflamasyona, konak savunmasına ve otoimmüniteye bağlı hücre fonksiyonlarının belli başlı programlarını aktive etmelerini sağlar. Fagosit aktivasyonu; hatırlamayı, hücre içine alımı ve antikor kaplı hedeflerin yıkımını kolaylaştıran stimülator Fcγ reseptörleri tarafından tetiklenir. Trombositlerdeki Fcγ reseptörlerine multivalan IgG’ lerin bağlanması trombosit agregasyonuna ve tromboza yol açar. Doğal katil hücreler üzerindeki Fcγ reseptörlerine IgG’ lerin bağlanması ise antikor kaplı hedeflerin sitotoksisitesi ile sonuçlanır.
IgE; mast hücrelerindeki, bazofillerdeki ve aktive olmuş eozinofillerdeki yüksek afiniteli Fcε reseptörlerine bağlanır. Fcγ reseptörlerinden daha düşük afinitelidirler. Fcε reseptörleri monomerik IgE’ leri bağlar. Tek bir mast hücresi üzerine birçok farklı antijen için spesifik olan IgE molekülleri bağlanmaktadır. Mast hücreleri gastrointestinal sistem, solunum sistemi mukozası ve derinin dermis tabakasının altında yer alır ve multivalan antijenlere yanıt için beklerler. Multivalan bazı antijenler (alerjenler), Fcε reseptörlerine bağlı yüzey IgE ile çapraz bağ kurar ve granüller içeren histaminin salınımına, sitokinlerin ve diğer inflamatuvar medyatörlerin salınımına neden olurlar. Normalde solunum, ürogenital, barsak epitelinde bulunan hücreler olan eozinofillerin IgE aracılıklı aktivasyonu, yüksek toksisitede granüle proteinlerin, serbest radikallerin ve prostoglandinler, sitokinler ve kemokinler gibi kimyasal medyatörlerin salınımına neden olur. Tüm bunlar sonucunda endotelyal hücreler aktive edilip, oratama eozinofiller ve lökositler çağrılır ve lokal inflamatuvar yanıt güçlendirilir.
Aktivasyon eşiğini ayarlayan ve stimülasyon sinyallerini sonlandıran inhibitör Fcγ reseptörleri efektör fonksiyonun regülasyonunda anahtar elementtirler. Bu tip inhibitör ve stimulatör Fc reseptörleri genelde aynı hücrede eksprese edilirler ve bu hücredeki spesifik stimulusa etkin yanıt, stimülatör ve inhibitör sinyaller aracılığıyla oluşur. İnhibitör Fcγ reseptörleri genelde, mast hücreleri üzerindeki Fcγ reseptörlerince tetiklenen immünolojik yanıtları ve immün kompleks birikme bölgelerindeki Fcγ reseptörleri aracılıklı inflamasyonu baskılamaktadır.
IgG ve IgM tarafından hedeflenen efektör aktivitelere, kompleman sisteminin bileşenleri de aracılık edebilir. Antijen bağlı multimerik immünoglobülin, antijen-antikor komplekslerinin ileri fagositozuna, artmış lokal vasküler geçirgenliğe ve inflamatuvar hücrelerinin çağrılmasına ve aktivasyonuna neden olarak, komplemanın klasik yolunun aktivasyonunu başlatabilir. Hasarın hedefi, antikor tarafından belirlenir ve hasarın kapsamı, immünoglobulinin ve komplemanın sinerjistik aktiviteleri tarafından belirlenir.
Antijen spesifik efektör T hücreleri doku hasarlarını başlatabilir. Uygun bir antijen ile karşılaşma sonrasında, hafıza T hücreleri; lokal endotel hücreleri, makrofajları ve diğer inflamatuvar hücreleri aktive eden sitokinleri ve kemokinleri salgilamak üzere uyarılırlar. T hücrelerinden çıkan sitokinler ile yönetilen efektör hücrelerle birlikte sitolitik T hücreleri doku hasarına aracılık etmektedirler.
Yardımcı T hücrelerden olan Th1 hücreleri hasara neden olacak şekilde IFN-γ üretirler ve makrofajları aktive ederler; oysa Th2 hücreleri IL-4, IL-5 ve eotaksin (eozinofil spesifik kemokin) üretirler ve eozinofillerin üstün olduğu inflamatuvar reaksiyonları tetiklerler.
Hipersensitivite Reaksiyonları
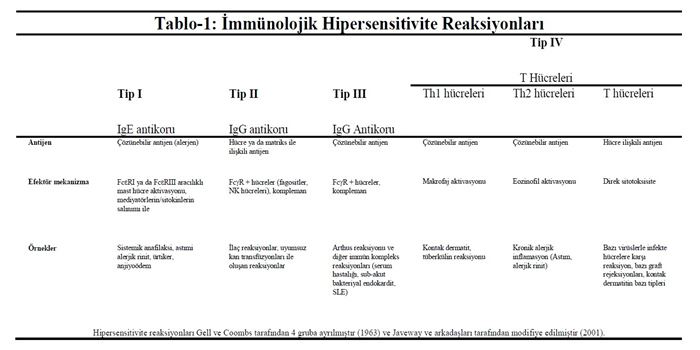
Yatkın bireylerde, zararsız çevresel antijenler, kazanılmış immün reaksiyonu, immünolojik hafızayı ve sonradan oluşan antijen maruziyetiyle inflamasyonu uyarırlar. Hipersensitivite ya da alerjik reaksiyonlar dediğimiz, bağışıklık sisteminin zararsız çevresel antijenlere (alerjenlere) gösterdiği bu aşırı reaksiyonlar doku hasarlarına yol açabildiği gibi, ciddi hastalıklara da neden olabilir. Hipersensitivite reaksiyonları kaynak aldıkları efektör mekanizmalara göre dört gruba ayrılırlar (Tablo-1). Tip I, II ve III hipersensitivite reaksiyonları için kullanılan efektör hücreler antikor molekülleridir; oysa tip IV reaksiyonlarda efektör hücreler antijen spesifik efektör T hücreleridir.
Otoimmün hastalıklar, hedef dokular üzerinde eksprese edilen self-antijenler için özgül antikorların ve T hücrelerin varlığı ile karakterizedir. Otoimmün hastalıklarda antijen tanıma mekanizmaları ve doku hasarlanmasına neden olan efektör fonksiyonlar, patojenler ve çevresel antijenlere reaksiyon ile ortaya çıkan mekanizmaları benzerlik göstermektedir. Bu mekanizmalar belli hipersensitivite reaksiyonlarını hatırlatır ve tablodaki gibi sınıflanır (Tablo-2). Hücre yüzeyine ya da ekstraselüler antijenlere karşı oluşan antikorlar tarafından neden olunan otoimmün hastalık Tip II hipersensitivite reaksiyonlarına; dokularda sonradan biriken çözülebilir immün komplekslerin oluşumu nedeni ile ortaya çıkan hastalık tip III hipersensitivite reaksiyonlarına ve efektör T hücreleri nedeni ile ortaya çıkan hastalık Tip IV hipersensitivite reaksiyonlarına örnek gösterilebilir. Tipik olarak, bu patojenik mekanizmalar birçok otoimmün hastalıkda aktif durumdadır.
TİP I HİPERSENSİTİVİTE REAKSİYONLARI

Tip I hipersensitivite reaksiyonları, IgE ile ilişkili bazı spesifik antijenlerin, mast hücreleri üzerinde bulunan ve mast hücre aktivasyonuna yol açan FcεR’ ler ile etkileşmesi sonucu başlamaktadır. Proteolitik enzimler ve histamin gibi toksik aracılar, daha önceden hazırda bulunan granüllerden hızla ortama salınırlar; aynı aktivasyon sonrasında kemokinler, sitokinler ve lökotrienler sentezlenirler. Bu mediyatörler vasküler geçirgenliği artırır; doku matriks proteinlerini yıkar; eozinofil üretimini ve aktivasyonunu sağlarlar (interlökin [IL]-3, IL-5, granülosit-makrofaj koloni uyarıcı faktör [GM- CSF]). Sonuç olarak; efektör lökositlerin bölgeye gelmesine neden olur (tümör nekroz faktör-α [TNF]-α, trombosit aktive edici faktör, makrofaj inflamatuvar protein [MIP – 1]), düz kasların kasılması, mukus salgısının uyarılmasına ve Th2 hücre yanıtlarının büyümesine (IL-4, IL-13) yol açarlar.
Hücre yüzeyi FcεR’ leri aracılığı ile aktive olan eozinofiller ve bazofiller hızla, yüksek derecede toksik granüler proteinler açığa çıkarırlar (major temel protein, eozinofil peroksidaz ve kollagenez). Daha uzunca bir süreç sonucunda da lokal inflamasyonu ve doku hasarlarını arttıran eozinofilleri, epitel hücreleri ve lökositleri aktive eden lökotrienleri, sitokinleri, prostaglandinleri, kemokinleri (IL-8) ve sitokinleri (IL-3, IL-5, GM-CSF) üretirler.
FcγR taşıyan efektör hücreler koordine bir biçimde hareket etmektedir. Mast hücreleri ürünleri tarafından başlatılan akut alerjik inflamatuvar reaksiyonlar ardında geç faz reaksiyonlar oluşur. Geç faz reaksiyonlar eozinofil, bazofil, Th2 hücre tipindeki lenfositlerin çağrılması ve aktivasyonlarından oluşmaktadır.
IgE aracılı reaksiyonların ortaya çıkmaları, mast hücresi aktivasyonunun konumuna bağlıdır. Mast hücreleri, vücut içerisinde vasküler ve epitel dokularda bulunmaktadırlar. Sensitize olmuş bir bireyde (antijenlere IgE reaksiyonu olan bir birey), mast hücrelerinin antijene tekrar maruz kalması sonucunda tip I hipersensitivite yanıtı ortaya çıkar. Deri altında bulunan mast hücrelerinin antijen ile uyarımı sonucu vasküler geçirgenlikte artış ve şişliğe (ürtiker ve anjioödem) sebep olurken, antijenlerin inhale edilmesi, bronşların daralmasına ve mukus salgısının artışına (astım ve alerjik rinit) ve antijenlerin yenmesi peristaltizm ve sekresyon (ishal ve kusma) artışına neden olmaktadır. Kan yoluyla alınan antijenler ise sistemik mast hücre aktivasyonuna, artmış lokal damar geçirgenliğine, hipotansiyona, doku şişliğine ve düz kasların kasılmasına neden olmaktadırlar ki tüm bu semptomlar sistemik anafilaksinin karakteristik özellikleridirler.
TIP II HİPERSENSİTİVİTE REAKSİYONLARI
Tip II hipersensitivite reaksiyonları, hücre yüzeyinin kimyasal modifikasyonu veya immün sistemin toleran olmadığı yabancı epitoplar oluşturan matriks bağlantılı antijenler tarafından meydana getirilir. B hücreleri bu antijenik değişime IgG üreterek karşılık verir. IgG bu modifiye hücrelere bağlanır ve onları kompleman aktivasyonuna, fagositoza ve antikora bağımlı sitotoksisite gibi zararlı olaylara duyarı hale getirir. Bu fenomen klinik olarak; ilaçlar, kan bileşenleriyle etkileştiğinde ve onların hücresel antijenlerini değiştirdiğinde görülebilir. Eritrositlerin immün aracılıklı zarar görmesi sonucunda ortaya çıkan hemolitik anemi ve trombositlerin zarar görmesi sonucu ortaya çıkan trombositopeni, her ikisi de tip II hipersensitivite reaksiyonları olup, belirli ilaçların yan etkileri sonucu ortaya çıkarlar. İnsan proteinlerinin bu şekilde modifikasyonu yeni epitoplar yaratır ve insanların ufak bir kısmında immün sistem tarafından yabancı antijen olarak algılanır ve bu kişilerde hücre yüzey proteini ve ilaç bileşenine karşı IgG ve IgM üretimini stimüle eder. Penisilin-spesifik IgG’ ler, kırmızı kan hücreleri üzerinde bulunan penisilin tarafından değiştirilmiş proteinlere bağlanırlar. Bu antikorların kan hücrelerine bağlanması, kompleman aktivasyonunu tetikler. Cl’ den C3′ e kadar kompleman aktivasyonu, C3b’ nin kırmızı kan hücrelerinin zarlarına kovalent bağlanması ile sonuçlanır. Bu bağlanma dolaşan kırmızı kan hücrelerini, dalak ve karaciğerde FcγR ve kompleman taşıyan fagositler tarafından fagositoza duyarlı kılar. Cl’ den C9′ a kadar olan kompleman aktivasyonu ve membran atak kompleksi oluşumu kırmızı kan hücrelerinin intravasküler olarak lizisine neden olur.
Bazı insanların ilaç aracılıklı tip II hipersensitivite reaksiyonlarına yatkın olmasına neden olan faktörler bilinmemektedir. Penisilin, kinidin ve metildopa bu mekanizma yolu ile hemolitik anemi ve/veya trombositopeni ile ilişkilendirilmiştir. Bir başka örnek ise heparine maruz kalan hastaların %1 ila 3′ ünde görülen, heparin ile meydana gelen, son derece ciddi ve yaşamı tehdit eden trombositopeni/tromboz komplikasyonudur.
Hücre yüzeyinde bulunan antijenlere ya da ekstraselüler matrikse yönlenen otoantikorlar; tip II hipersensitivite reaksiyonlarında görülen mekanizmalara benzeyen mekanizmalar aracılığıyla doku hasarına neden olmaktadırlar. Otoimmün hemolitik anemide, eritrositlere karşı oluşan IgG ve IgM antikorları hücre hasarlarına neden olur; çünkü opsonize hücreler (IgG ya da IgM ve kompleman ile kaplanan hücreler) karaciğerde ve dalaktaki fagositlerce dolaşımdan temizlenir veya membran atak kompleksinin oluşumuyla lizise uğrarlar. Otoimmün trombositopenik purpurada görülen trombosit hasarı da benzer bir mekanizmayla meydana gelir. Çünkü çekirdekli hücreler, hücre zarı sınırlı kompleman düzenleyici proteinleri eksprese ederler; bunlar hücre zarı atak kompleksi ile çözülmeye daha az duyarlıdırlar; fakat antikorla kaplandığında, fagositoz veya antikorlara bağımlı sitotoksisite için hedef haline gelirler. Bu mekanizma, otoimmün ve alloimmün nötropeniden de sorumludur. Hücre içindeki antijenleri ya da hücre dışı antijenleri tanıyan IgM ve IgG antikorları, FcR’ ler ve kompleman mekanizmaları aracılığı ile lokal inflamatuvar hasara yol açarlar. Pemfigus vulgaris, desmoglein (epidermal keratinositlerin hücre içi adezyon yapı parçası)’ in hücre dışı parçalarına yönelen otoantikorlarla oluşan adezyon kaybı nedeni ile keratinositlerde meydana gelen son derece ciddi bir hastalıktır. Tip II hipersensitivite reaksiyonlarına başka bir örnek ise Goodpasture hastalığıdır. Bu hastalıkta Tip IV kollajenin (bazal membrandaki kollajen) α-zincirine yönelen antikorlar, glomerüler ve akciğer bazal membranda birikir. Doku sınırlı antikorlar; proteazların, reaktif oksidanların, sitokinlerin ve prostoglandinlerin serbestleşmesini başlatarak, FcR’ ler aracılığı ile monositleri, nötrofilleri ve bazofilleri aktive ederler. Komplemanın özellikle de C5a’ nın lokal aktivasyonu, inflamatuvar hücreleri çağırır ve aktive eder böylece doku hasarını artırır. Membran atak komplekslerinin bir araya gelmesi veya FcR tarafından başlatılan antikor bağımlı sitotoksisite ile komşu hücreler lizise uğratılırlar.
Hücre yüzey reseptörlerine karşı gelişen otoantikorlar reseptör fonksiyonunu uyararak ya da bloke ederek hastalığa yol açabilirler. Myastenia graviste, iskelet kası hücrelerinde bulunan asetilkolin (Ach) reseptörlerine karşı oluşan otoantikorlar, reseptöre bağlanırlar, reseptörün lizozomlarda internalizasyonuna ve bozulmasına neden olarak nöromusküler geçiş etkinliğinin azalmasına ve ilerleyen kas güçsüzlüğüne yol açarlar. Bu tip hastalık mekanizmasının tersi olarak; Graves hastalığı, agonist olarak davranan otoantikorlar ile karakterizedir. Tiroid stimüle eden hormon reseptörlerine bağlanan otoantikorlar, doğal ligand gibi davranarak gereğinden fazla tiroid hormonunun üretilmesine neden olurlar, geribildirim düzenini bozarlar ve sonuçta da hipertiroidizme neden olurlar.
TİP III HlPERSENSİTİVİTE REAKSİYONLARI
Tip III hipersensitivite reaksiyonları, antijen içeren küçük ve çözünebilir immün komplekslerin dokularda birikmesi ve bu antijenlere yönelen yüksek afiniteli IgG antikorlar ile meydana gelir. İmmün komplekslerin lokalize birikimleri FcR taşıyan mast hücrelerini ve fagositleri aktive eder, kompleman kaskadının ve doku hasarının tüm efektörlerini harekete geçirir.
İmmün kompleksler, tüm antikor reaksiyonlarında meydana gelir. Bununla beraber, immün komplekslerin oluşumu ve kaderi, antijenin ve antikorun biyofiziksel ve immünolojik özelliklerine bağlıdır.
Bu özellikler:
1. Antijenin boyutlarını, net yüklerini ve değerliklerini;
2. Antikorun sınıfını ve alt sınıflarını;
3. Antijen-antikor etkileşimini afinitesini;
4. Antikorun net yükü ve konsantrasyonunu;
5. Antijenin ve antikorun molar oranlarını ve
6. İmmün kompleksin kompleman sisteminin proteinleri ile etkileşim yeterliliğini içermektedir.
İmmün kompleksin büyüklüğü, antijenin fiziksel büyüklüğü, değerliği, o antijene ait olan antikorun bileşim sabiti, antijenin ve antikorun molar oranları, reaktanların mutlak konsantrasyonları tarafından etkilenmektedir. Daha büyük agregatlar komplemanı daha etkin bir biçimde fikse ederler, FcR’ lerin ve komplemanın bağlanabileceği daha geniş ve çok değerlikli ligandlar dizisi oluştururlar, dalak ve karaciğerdeki fagositler tarafından dolaşımdan daha hızla uzaklaştırılırlar. Bir immün yanıtın erken safhalarındaki antijen fazlalığında oluşan daha küçük immün kompleksler kan içinde sirküle olup; FcR’ ler ve kompleman reseptörleri ile etkileşimleri sonucu meydana gelen inflamatuvar reaksiyonları ve doku hasarını başlattıkları kan damarlarında birikirler.
Arthus reaksiyonu, lokalize tip III hipersensitivite reaksiyonlarına iyi bir örnektir. Arthus reaksiyonu sensitize oldukları antijenlere karşı IgG antikorlarına sahip olan bir bireye çözünebilir bir protein antijeninin subkutan enjeksiyonu sonucunda ortaya çıkmaktadır. Lokal immün kompleksler oluşur, mast hücrelerindeki ve fagositlerdeki FcR’ lere bağlanırlar. Böylece vasküler geçirgenliği arttıran, iç akıma ve lökositlerin aktivasyonuna bunların da ötesinde zararın artmasına neden olan inflamatuvar mediyatörlerin serbestleşmesine neden olurlar.
Ayrıca, kompleman da aktive edilir ve inflamasyonun büyümesine yol açar.
Tarihsel olarak ilk kez bakteriyel infeksiyonların tedavisinde, terapötik at anti-serumu verilen bireylerde tanımlanan serum hastalığı, sistemik bir tip III hipersensitivite reaksiyonu örneğidir. Serum hastalığı genel olarak, büyük miktarda çözünebilir antijenin enjeksiyonu sonucunda meydana gelir. Klinik özellikler, üşüme, ateş, döküntü, ürtiker, artrit, glomerulonefrit gibi belirtilerden oluşur. Hastalık belirtileri; antikorlar, yabancı proteinlere karşı birleşip sirkülasyon halindeki antijenler ile beraber immün komplekslerini oluşturduğu zaman; yani antijenle karşılaşmadan sonraki 7 ila 10 gün içinde ortaya çıkmaktadır. İmmün kompleksler, fagositleri ve komplemanı aktive ettikleri kan damarlarında birikerek yaygın doku hasarına ve klinik semptomlara neden olurlar. Bununla beraber, bu etkileri geçicidir ve antijenler temizlendikçe sorun çözümlenmiş olur.
Serum hastalığına benzer bir sendrom, patojenlerin devam eden immün reaksiyonların üzerinde persiste ettiği, kronik infeksiyonlarda da meydana gelmektedir. Sub-akut bakteriyel endokarditte, antikor üretimi devam etmektedir; fakat bu antikor üretimi infeksiyöz mikropları yok etme konusunda başarısız olmaktadır. Patojenler yeni antijenler oluşturarak çoğaldıkça dolaşımda immün kompleksler oluşmakta ve küçük kan damarlarında; deri, böbrekler ve sinirlerin inflamatuvar hasarına neden olarak birikmektedirler. Hepatit B virüsü infeksiyonu, antijen artımının fazla olduğu, hastalığın ilk dönemlerinde, immün kompleks birikimi ile ilişkili olabilir; çünkü bu dönemde hepatit B yüzey antijenine karşı geliştirilen antikor üretimi henüz yetersizdir ve bazı an-ikterik hastalarda akut artrit gözlenmektedir. Hepatit C viral infeksiyonu ile ilişkili olabilecek mikst kriyoglobulinemi de immün kompleks aracılıklı bir vaskülittir. IgG, IgM ve hepatit C antijenleri içeren immün komplekslerin birikmesinin; periferal sinirlerde, deride ve böbreklerde inflamasyona neden olduğu bir hastalıktır. Rejeksiyonu önlemek için, insan T hücrelerine özgü fare monoklonal antikorlarının kullanıldığı transplant alicilarında da, trombolizise sebep olan streptokinaz ile tedavi edilen myokardiyal infarktüs hastalarında da serum hastalığı oluşabilir.
Prototipik immün kompleks aracılıklı otoimmün bir hastalık olan sistemik lupus eritematozus, hücresel bileşenlere (tipik olarak DNA ve DNA bağlayan proteinlere) karşı oluşan sirkülasyon halindeki IgG ile karakterizedir. Küçük immün kompleksler; FcyR’ ler ile birlikte lokal doku hasarlarının başlatılmasında baskın bir rol oynayarak; deride, eklemlerde ve glomerüllerde birikirler.
TİP IV HİPERSENSİTİVİTE REAKSİYONLARI
Geçikmiş tipte hipersensitivite reaksiyonları olarak da bilinen, Tip IV hipersensitivite reaksiyonları, antijen spesifik efektör T hücreleri aracılığıyla meydana gelir. Diğer hipersensitivite reaksiyonlarından, antijenle karşılaşılmasından duyarlılık reaksiyonun gerçekleşmesine kadar geçen sürenin uzunluğu (1 ile 3 gün) ile ayrılır. Antijenler alınır, işlenir ve makrofajlar veya dendritik hücreler tarafından sunulur. Spesifik antijenleri tanıyan Th1 efektör hücreleri (bunlar az bulunur ve gelmeleri zaman alır), makrofajları aktive eden kemokinleri ve doku hasarlarında aracılık yapan sitokinleri salgılamak üzere uyarılırlar. IFN-γ; makrofajları aktive eder ve makrofajların inflamatuvar medyatörleri salgılamasını artırır. Bu arada TNF-α ve TNF-β endotel hücreleri aktive eder, vasküler geçirgenliği artırır ve lokal dokulara hasar verirler.
Prototip tip IV hipersensitivite reaksiyonu tüberkülin testidir; fakat kontakt duyarlanmaya neden olan antijenler (zehirli sarmaşık, belli metaller vb.) ile de benzer reaksiyonlar meydana gelir ve eritem, hücresel infiltrasyon ve veziküllerle karakterize epidermal reaksiyonlar oluşur. CD8+ T hücreleri, direk toksisite yoluyla da hasara aracılık edebilirler.
Efektörlerin makrofaj olduğu Th1 aracılı hipersensitivite reaksiyonlarının aksine, Th2 aracılı hipersensitivite reaksiyonlarında, eozinofiller hakimdir. Th2 efektör T hücreleri, kronik astımda doku hasarları ile ilişkilidir. Th2 hücreleri, eozinofilleri hazırlamak ve aktive etmek için sitokin (IL-5 ve eotaksin) üretirler, böylece eozinofillerin degranülasyonuna ve bunun da ötesinde doku zedelenmesine ve geri dönüşü olmayan kronik hava yolu hastalıklarına öncülük ederler.
Bazı otoimmün hastalıklarda efektör T hücreleri, self antijenleri özellikle fark ederler. Hem direk sitotoksisite yolu ile hem de aktive edilmiş makrofajlar aracılı inflamatuvar reaksiyonlar yolu ile doku hasarına neden olurlar. Tip I insülin bağımlı diabetes mellitusta; T hücreleri, pankreatik β adacık hücrelerinin yıkımına aracılık ederler. Myelin temel proteinlerine özgü IFN-γ üreten T hücreleri multipl sklerozda saptanmıştır. Romatoit artrit kısmen de olsa aktive edilmiş Th1 hücrelerinin neden olduğu diğer bir otoimmün hastalıktır.
Sağlıklı günler dileğiyle…
Prof. Dr. Cengiz KIRMAZ

