Alerjik ve Non-alerjik Rinitte Patogenezden Tedaviye
Solunum sistemi; bireyin son nefesini verinceye kadar atmosferle ilişkisini sağlayan organlar topluluğu olarak tanımlanabilir. Bu sistem; solunan havayı filtreleme, ısıtma, oksijen alımı ve kandan karbondioksitin uzaklaştırılması gibi önemli görevleri üstlenir. Sistem direkt dış ortam ile bağlantılı olduğundan tahammül sınırları son derece geniş olarak yaratılmıştır. Ancak bu noktada bazen patojenler ve alerjenler sistemi ağır bir şekilde zarara uğratıp, morbidite ve mortaliteye neden olabilirler. Solunum sistemi bu anlamda bakıldığında, yaşamsal özelliğe sahip ve yeri doldurulamayacak bir sistem olarak görülmektedir.
Solunum sistemi ile ilgili sık görülen hastalıklar değerlendirildiğinde rinit ve astım ilk iki sırada yer almaktadır. Rinit nazal kavite mukozal yapısının ciddi etkilendiği, hapşırma, burun tıkanıklığı, burun akıntısı ve burun kaşıntısı semptomları ile giden iltihabi bir hastalıktır. Hastalığı çok genel olarak enfeksiyon kaynaklı ve enfeksiyon dışı patogeneze sahip iki grupta inceleyebiliriz. Enfeksiyon dışı patogeneze sahip en sık karşılaştığımız rinit şekilleri “alerjik rinit (AR)” ve “non-alerjik rinit (n-AR)” olarak tanımlanabilir. AR; alerjenlerin tetiklediği, inflamatuvar hücreler ve bazı inflamatuvar mediyatörlerin (sitokinler ve nörotransmiterler gibi) rol aldığı, sensoriyal sinir uçlarının etkilendiği, kapiller kaçak ve venöz sinüzoidlerde ödemin ortaya çıktığı nazal mukozal iltihabi durum olarak tanımlanabilir. Hastalık genellikle ergenlik ve genç erişkin yaşlarda görülmekle birlikte her yaşta ortaya çıkabilmektedir.
Alerjik rinit tipleri, etiyoloji ve semptomları
AR, Klinik olarak genellikle mevsimsel alerjik rinit (SAR) ve yıl boyu süren (perennial) alerjik rinit (PAR) olarak iki büyük gruba ayrılmaktadır. SAR ot, hububat, yabani ot ve ağaç polenleri gibi mevsimsel alerjenlerin tetiklemesi ile ilişkili olup; bu alerjenlere duyarlı bireylerde burun akıntısı, hapşırma, burun kaşıntısı, bazen burun tıkanıklığı; ek olarak göz (göz de yanma, sulanma ve kaşınma gibi), boğaz ve kulak kaşıntısı semptomları ile göze çarpar. PAR ise daha daha çok ev tozu akarı, hayvansal kaynaklı ve küf mantarı alerjenlerine duyarlı kişilerde bu bulguların yıl boyu sürmesi şeklinde karşımıza çıkar. Ancak hastalık son dönemde daha sıklıkla “intermitant” ve “persistant” rinit olarak kategorize edilmektedir. Şikayetlerin haftada 4 günden fazla sürdüğü veya ardışık 4 haftadan daha fazla devam ettiği durumlar persistant rinit olarak tanımlanmaktadır. Buna ek olarak; şikayetler kişinin günlük aktiviteleri, spor, eğlence, iş, okul ya da uyku faaliyetlerinin hiç birini etkilemiyorsa “hafif”; eğer bunlardan bir veya daha fazlası etkiliyorsa “orta-ağır” şeklinde tanımlanır.
Alerjik rinitin patofizyolojisi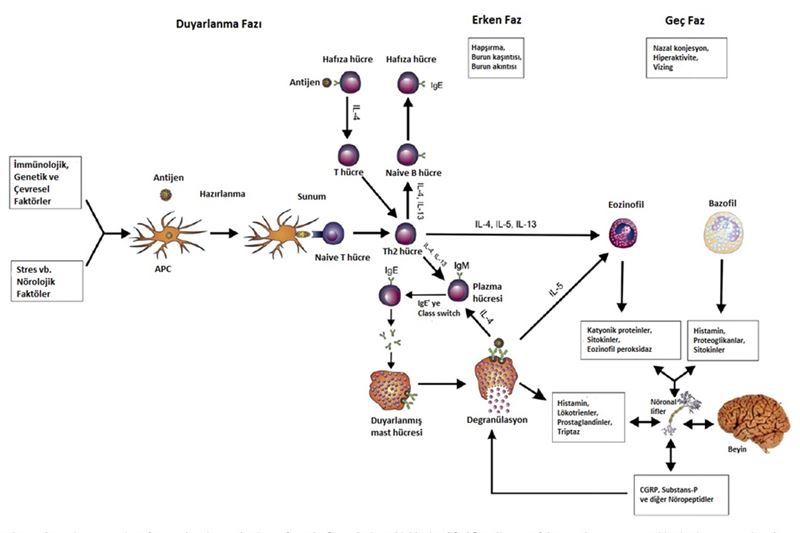
Duyarlanma ve erken fazÜst solunum yolu mukozamızda yoğun bir şekilde, ancak heterojen tipte antijen sunan hücre (APC)’ ler bulunur. Monosit, makrofaj ve dentritik hücreler bunların başlıcalarıdır. B hücreler daha nadir olarak bulunmaktadırlar. Dentditik hücreler bunlar içinde immünolojik cevabı başlatan en önemli APC’ lerdir. Solunum yolunda karşılaşılan antijenler APC tarafından alınır, küçük aminoasit dizgelerine kesilerek MHC sınıf II molekülleri ile T lenfoistlere sunulurlar. Buradaki T lenfositler atopik kişilerdeki IL-4 varlığında naive T lenfositlerden Th2 lenfositlere dönüşmüş formlardır. Bu Th2 tipindeki hücreler de bilindiği üzere daha çok IL-4 ve IL-13 gibi sitokinler üretip salgılayabilen hücrelerdir. IL-4 ve IL-13 sitokinlerinin B lenfositlerden IgE sentezi yaptırdığını da biliyoruz. Nitekim bu sitokinler plazma hücrelerine dönüşmüş olan B lenfositteki IgM’ yi IgE’ ye class switch’ e zorlarlar. Oluşan bu antijen spesifik IgE, mast hücrelerinin yüzeyindeki yüksek afiniteli reseptörleri olan FcR1’ e otururlar. Bu bağlanma irrevesibl bir bağlanmadır. Buraya kadar oluşan olayların toplamı “duyarlanma” olarak adlandırılır. Aynı antijenle tekrar karşılaşıldığında bu antijene spesifik olan iki ya da daha fazla IgE antijen aracılığı ile köprüleşince FcR1’ in hücre içi parçacıklarında bir takım aktivasyon süreçleri sonucunda mast hücrelerinde hazırda bulunan granüllere degranülasyon sinyali verilmiş olur. Bu aşamadan sonra alerjik inflamasyonun erken mediyatörleri olan, granüllerde hazırda bulunan histamin, triptaz gibi moleküllerle birlikte aynı anda hızla mast hücresinden üretilen bazı inflamatuvar mediyatörler ortama salınırlar ki tüm bu mediyatörler burunda kaşıntı, su gibi akıntı ve hapşırma gibi şikayetlerden sorumludurlar. Biz bu olaya alerjik reaksiyonun “erken faz”ı diyoruz.
Geç faz reaksiyon
Geç faz reaksiyonun başrol oyuncuları, Th2 hücreler, eozinofiller, bazofiller, nötrofiller ve bunların salgıladıkları bazı sitokinlerle diğer aracı moleküllerdir. Eozinofiller bu reaksiyonda en önemli rolü oynarlar. Salgıladıkları süperoksit anyonları ve hidrojen peroksit gibi radikallerle epitelyal hasara neden olurlar. IL-5, eotaksin gibi eozinofil kemoatraktanları, eozinofil katyonik protein (ECP), major bazik protein ve eozinofil kaynaklı nörotoksin gibi eozinofil granüler ürünleri nazal hiper-reaktivitede önemli rol oynarlar. Bu proteinler aynı zamanda ciddi havayolu epitelyum hasarı yaratıp lokal sinir uçlarını da etkileyebilirler. Bu etkilenme sonucunda, sinir uçlarından açığa çıkan nöropeptidlerin yıkılımını sağlayan endopeptidaz aktivitesinde de aksama meydana gelir ve bu nöropeptidlerin inflamatuvar süreçte uzunca etkili olmalarına yol açılır. Mast hücrelerinden degranülasyon ardından hızla sentezlenmeye başlayan PGD2, löktrien C4, PAF, sitokinler, eozinofil kemotakrtik faktör gibi mediyatörler ile inflamasyon alanına nötrofil ve eozinofiller çekilmektedir. Bu esnada orkestra şefi olan Th2 hücreleri tarafından IL-3, IL-4, IL-5, IL-13 gibi sitokinlere ortama salınmaktadır. IL-4 ve IL-13, fibroblastlardan RANTES, eotaksin, membran ko-faktör protein ve ECP yapımını stimüle eder. Fibroblastlardaki IgE reseptörlerininb aktive olmasıyla da plazma membranı dergade olur ve lökotrien ve prostaglandin üretimi sağlanır. Lökotrienler ortama eozinofil çekerler, mikrovaküler kaçak nedeniyle ödeme sebep olurlar, mukus sekresyonunu artırırlar ve ayrıca da kinin yolağını da aktive ederler. Th2 hücrelerinden salınan sitokinlerin etkisi ile vasküler endotalde artan ICAM-1, VCAM-1, E-selektin ekspresyonu nedeni ile eozinofiller, damar duvarına tutunup, damar dışına çıkar ve enflamasyon bölgesine göç ederler. IL-4’ e cevaben inflamatuvar hücrelerden üretilen TNF-α, bazı özel lenfozit tiplerinde VCAM-1 gibi adezyon moleküllerinin ekspresyonunu artırarak bu lökositlerin adezyon ve aktivasyonuna neden olur. Aynı şekilde bu sitokinlerin sinerjistik etkisi ile endotelyal hücreler aktive olur ve uzamış endotelyal VCAM-1 ekspresyonu sağlanır. Sonuçta bu mekanizmalarla ortaya çıkan geç faz reaksiyonun semptomları olarak nazal konjesyon, nazobronşiyal hiperreaktivite ve kronik vizing oluşmaktadır.
Alerjik rinit patofizyolojisi ile nörojenik yolakların ilişkisi
Nörotransmitterler oluşturdukları sekresyon artışı, düz kas tonüs değişiklikleri, vazodilatasyon ve hücre toplanması gibi etkileri ile AR patogenezinde önemli rol oynarlar. Burada nörojenik mediyatörlerin oluşturduğu fenomen “nörojenik inflamasyon” olarak adalndırılır. Nörojenik yolakların AR ve astımda semptomatik olarak öksürük ve hapşırma refleksinde önemli olduklarını biliyoruz. Mast hücreleri gibi alerjik inflamasyonun efektör hücrelerinin nörolojik mekanizmalarla iki yönlü ilişki içinde olduğunu görmekteyiz. Mast hücrelerinden salınan histamin afferent sinir uçlarından nöropeptid salınımını aktive etmektedir, ardındansa nörotransmitterler nedeniyle mast hücreden mediyatör liberasyonu artırılmaktadır. Bradikinin, PGE2, LTD4, MBP, ECP, IL-1, TNF-α gibi diğer mediyatörlerle de nöronal hipereksitabilite oluşmaktadır.
Üst hava yollarındaki submukozal bezler, damalar ve epitelyum peptiderjik nöronlarca innerve edilmektedir. Kapsaisin ile yapılan çalışmalar hem rinit hem de astımda nöropeptidlerin rolünü anlamamıza yardımcı olmuştur. Kapsaisinin tekrarlayan uygulamaları ile aktive olan vanniloid reseptörler sayesinde AR’ deki semptomların ortadan kaldırıldığı gözlenmiştir. Ancak kapsaisinin akut uygulamaları ardından nazal mukozal sensoriyal sinir uçlarının aktive olduğu ve Substans P (SP) ve kalsitonin gen bağımlı peptid (CGRP) salgılandığı, ardından da burunda yanma, konjesyon ve burun akıntısı semptomları oluştuğu gözlenmiştir. Deneysel hayvan araştırmalarında, nazal kavite içine histamin uygulanması sonrasında SP indüksiyonu olduğu gözlenmiştir. Yine hayvan çalışmalarında alerjen provokasyonu ile SP, nörokinin A, VİP diğer nörotransmitterlerin salındığı saptanmıştır. Erken fazda oluşan semptomlardan hapşırmanın frekansı ile SP arasında bir korelasyon olduğu gösterilmiştir. SP, havayolu inflamasyonunda önemli rolü olan IL-1’ indüklemektedir. SP’ nin NK1 reseptörlerine bağlanmasının stres sinyal iletisi oluşumu, ağrı ve düz kas kasılması ile inflamasyonun ortaya çıkışı arasında paralellik gösterilmiştir. Aynı şekilde NK1 resptör aktivasyonu sonucunda hava yollarında mukozal sekresyon artışı, ekstravazasyon, bronşiyal konstrüksiyon olduğu saptanmıştır. Tedavi amaçlı kullanılan steroidlerin nöropeptid sentezini ve taşikinin reseptör ekspresyonunu inhibe ederek faydalı olduğu da gösterilmiştir.
Sinir büyüme faktörü (NGF) nin kemik iliğinden eozinofil ve bazofil hücre diferansiyoasyonu ve büyümesi için önemli bir faktör olmasının gösterilmesi de AR’ deki nörojenik komponent için bir kanıt olabilir. Ayrıca, kronik AR’ de de nazal alerjen uyarımı sonrasında da nazal yıkama sıvılarında NGF düzeylerinin artığı gösterilmiştir.
Tüm bu bulgularla, AR’ de nöral ve inflamatuvar mekanizamaların iç içe olduğunu söyleyebiliriz. Sonuç olarak; “AR, nörojenik ve hücresel inflamasyonun sonucu ortaya çıkan bir durumdur” şeklinde yorumlanabilir.
Non-alerjik rinit patogenezi
n-AR, alerjik rinit semptomlarının gözlendiği ancak herhangi bir alerjik patogeneze ait kanıtın (deri testi pozitifliği ve/veya serum spesifik IgE) bulunamadığı durumlar olarak tanımlanır. n-AR olarak tanımlanan klinik durumlar Tablo-1’ de gösterilmiştir.
Non-alerjik (non-infektif) rinitler/Rinopati
1. İdiyopatik rinitler (Vazomotor rinit)
2. Eozinofili ile seyreden non-alerjik rinit (NARES)
3. Östrojenle indüklenen rinitler (Gebelik, mestrüel siklüsla ilgili, Konrseptiflerle ilgili)
4. Atrofik rinit
5. Gustatuvar rinit (Baharatlarla indüklenen)
6. Soğuk hava ile indüklenen (Kayakçı burnu)
7. Anatomik anormallikler nedeniyle oluşan rinitler
8. Sistemik hastalıklarla ilişkili rinitler (Vaskülitler, granülomatoz hastalıklar)
Yukarıdaki sınıflamadan da anlaşılacağı gibi n-ARin patofizyolojisi son derece heterojendir. En sık görülen durum idiyopatik olarak da dalandırılan “vazomotor rinit” tir. Hastalarda bir enfeksiyon, sinüzit ya da polip, her hangi bir anatomik anormallik yanında alerji kanıtı da bulunmamaktadır. Bu kişilerin nazal semptomları, mevsimsel patern göstermeyen, daha çok burun tıkanıklığı, burunda su gibi akıntı yanında nadiren burun kaşınması ve hapşırma bulguları şeklindedir. Alerjik rinitlilerden daha az olmakla birlikte aile hikayeleri vardır. Semptomlar atmosferik durumla yakından ilikili gibi görünmektedir. Nazal steroidlere ortalama bir cevap alınmaktadır. Topikal antihistaminik olarak kullanılan azelastine alınan cevap nedeniyle patofizyolojisi hakkında ilginç hipotezler öne sürülmüştür. Bir yandan da bu hastaların ¼ kadarında uzun süreli takipte, ilerleyen dönemlerde alerjik rinit kanıtları gözlenebilmektedir. Bu vakalar üzerinde yapılan gözlemsel çalışmalar sonucunda patofizyolojik alt yapı hakkında bazı bilgiler edinilmiştir. Örneğin nöral fonksiyon anormalliklerinden bahsedilmektedir. Bu hastalarda soğuk hava provokasyonu sonucu ciddi bir aşırı duyarlılık gözlenmiştir. Bunun dışında nazal nosiseptör C-liflerini defonksiyone eden kapsaisinin tekrarlayan burun içi uygulamaları sonucunda neredeyse altı aya yakın semptomlarda düzelme ve ayrıca soğuk hava porovokasyonuna cevapsızlık sağlanabildiği için patogenezin daha çok nörojenik mekanizmalara bağlı olduğu düşünülmektedir. Bu hastalarda mukozal inflamasyon olmaması nedeniyle de “rinit” teriminden daha ziyade “rinopati” terimini kullanmak daha doğru olacaktır.
Bunun dışında son dönemlerde “lokal alerjik rinit” diye tanımlanan bir grup vardır. Bu grup daha önceleri NARES olarak adlandırılmaktaydı. Burun içi mukozalarında inflamatuvar hücrelerin (eozinofil ve bazen mast hücreleri) bolca bulunabildiği gösterilen bu hastalarda alerjenlerle yapılan deri testlerinde pozitiflik ve/veya serum sepesifik IgE saptanamamasına rağmen, bazı alerjenlerle nazal ya da oral provokasyon pozitif saptanmaktadır. Ayrıca bu hastalarda alerjen uyarısı sonrası erken dönemde nazal sekresyonlarında mast hücre aktivasyon göstergesi olan triptaz, eozinofil aktivasyon göstergesi olan ECP düzeylerinde artış saptanmaktadır. Yine bu hastaların nazal sekresyonlarında reaksiyon verdikleri alerjenlere spesifik IgE saptanabilmektedir.
Alerjik rinit ve non-alerjik rinit tedavisinde bu patogenetik mekanizmaları göre hedefler
1- Alerjen ya da tetikleyicilerden uzak durmak,
2- Uygun farmakoterapi ajanları kullanmak,
3- Hastayı immünoterapi açısıdan değerlendirip, uygunsa immünoterapi yapmak,
4- Hasta eğitimi ve takip.
Alerjen kaçınma pratik olarak her zaman çok kolay olmasa da AR tedavisinin vazgeçilmezlerindendir. Hastanın deri testlerinde kendine özel saptanmış olan duyarlı alerjenlerinden maksimal düzeyde kaçınması şarttır.
Farmakoterapi
AR ve n-AR’ de semptom kontrolü ve yaşam kalitesinin artırılması açısından ilk tedavi modalitesi “farmakoterapi” dir. Şu anki farmakolojik tedavi hedefleri, aktive hücrelerden mediyatör salınımını ve bunların end-organ etkilerini inhibe etmek üzerine kurulmuştur. Ancak maalesef tek bir mediyatörü inhibe etmek ile bu sonuca varmak neredeyse olanaksızdır. Bu nedenle ilaçlar daha çok kombinasyonlar şeklinde uygulanmaktadır. AR’ de kullanılan önemli farmakolojik ajanlar: antihistaminikler, kortikosteroidler, antilökotrienler, dekonjestanlar, mast hücre stabilizatörleri ve antikolinerjikler olarak sınıflanabilirler. Farmakolojik ajanlarla elde edilmeye çalışılan etkiler Şekil-2’ de özetlenmeye çalışılmıştır.
Antihistaminikler
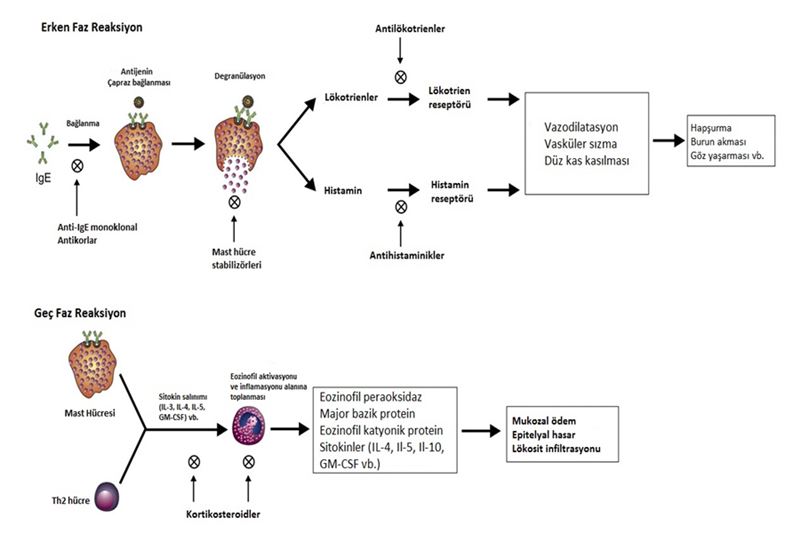
Antihistaminikler, H1 reseptörlerine yarışmalı olarak bağlanan moleküllerdir. Vasküler permeabilite, düz kas kasılması ve kaşıntı hissini azaltarak, hapşırma, burun akması ve burun kaşınmasını tedavi etmemize yardımcı olurlar
Birinci jenerasyon antihistaminikler ucuz olmalarına rağmen ciddi santral sinir sistemi penetrasyonu olduğunu biliyoruz. Bu nedenle maalesef nerdeyse hastaların %10-40’ ında ciddi dikkat dağınıklığı, uyku hali ve konsantrasyon bozukluğuna sebep olmaktadırlar. Mukozal membranlarda kuruluk, üriner retansiyon, konstipasyon, taşikardi, görme netliğinde azalma gibi anti-kolinerjik yan etkiler yaşlı hastalarda bu ilaçların kullanımını oldukça fazla kısıtlamaktadır. Ayırca uzun süreli kullanımı gereken bu ilaçların serotonin reseptörleri ila ilişkili antagonistik etkileri maalesef kilo alımına neden olabilmektedir. Trefenadin ve astemizol ilk 2. jenerasyon antihistaminikler olup santral sinir sistemi penetrasyonları eski jenerasyona göre daha azdır; ancak, duyarlı hastalarda oluşturdukları aritmi nedeniyle klinik prtaikte kullanımdan kaldırılmışlardır. Loratadin ve setirizin genellikle daha az sedasyon yapan yeni jenerasyon ilaçlardandır. Levosetirizin, setirizin molekülünün bir enantiomeri olup, etkili olduğu dozlarda maalesef sedasyona neden olmaktadır. Feksofenadin, terfenadinin; deslarotadin de loratadin in aktif metabolitleridir; bunlar bazen 3. jenerasyon antihistaminikler diye adlandırılmaktadırlar. Feksofenadinin kan beyin bariyerini geçmediği ve bu nedenle sedasyon yapmadığı bildirilmektedir. Ancak klinik kullanımda maalesef durumun böyle olmadığı görülmektedir. Desloratadinin de daha sedasyon ve anti-kolinerjik yan etkiye sahip olduğu bildirilmektedir.
Son dönemde antihistaminiklerin antiinflamatuvar etkilerinden bahsedilmektedir. Mast hücre ve bazofilleri, kalsiyumun transmembran geçişi ve intrasellüler cAMP’ yi inhibe ederek reseptör bağımsız olarak stabilize ettikleri ve böylece histamin, triptaz ve prostaglandin gibi inflamatuvar mediyatörlerin salınımını azalttıkları belirtilmektedir. Ancak, bir çok antihistamin maalesef terapötik dozlarda bu hücrelerde stabilizasyon yapamamaktadır. Ketotifen, olopatadin, azelastin, bepotastin ve alkaftadin ise daha çok hem H1 reseptör antagonisti hem de mast hücre stabilitesi olan dual etkili antihistaminikler olarak bilinmektedirler. Bazı antihistaminlerin H1 reseptör aracılığı ile NF-B ve GATA3 transkripsiyonunda inhibisyon yaptığı ve anti-inflamayuvar etkiyi bu sayede gerçekleştirdiği belirtilmektedir.
Kortikosteroidler
Kortikosteroidler, bir çok inflamatuvar hastalığın tedavisi açısından en iyi bildiğimiz birinci basamak anti-inflamatuvar ilaçlardır. Kortikosteroidlerin çok bilindik yan etkileri olmasına rağmen halen en önemli farmakolojik ajanlardan biri olduğunu görüyoruz. Çocuklarda büyüme geriliği yanı sıra tüm vakalarda metabolizma bozulmaları, glokom ve katarakt formasyonu, immünsüpresyon, HPA aksının süpresyonu, ciltte incelme, davranış bozuklukları, osteoporoz gibi yan etkiler en sık karşılaştıklarımızdır. Sistemik kullanımda ortaya çıkan bu kısıtlamalar nedeniyle AR’ de daha çok intranazal olarak kullanımı ön plana çıkmıştır. Birinci basamak tedavide intranazal preparatlar içinde içinde şu an için en çok kullanılan farmakolojik ürünlerdir. Halen kortikosteroidlerin anti-inflamatuvar mekanizmaları çok net olmamasına rağmen en önemli etkileri sitokin ve kemokin inhibisyonu olarak görülmektedir. Sitoplazmadaki glukokortikoid reseptörleri (GR)’ ne bağlanıp, dimerize olurlar ve nükleusa geçerler; ardından glukokortikoid response element (GRE) ile ilişkiye geçer ve sonuç olarak lipokortin-1, IL-10, IL-1 reseptör antagonisti ve nötral endopeptidaz gibi anti-inflamatuvar proteinlerin gen kodlarının transkripsiyonlarını artırırlar.
Glukokortikoidler nazal lavaj sıvısında hatırı sayılır bir biçimde inflamatuvar hücre sayısında da düşme sağlarlar. Özellikle eozinofil sayılarında belirgin azalma meydana getirirler. Bu durumu hem IL-5 hem de GM-CSF üzerindeki inhibitör fonksiyonları sayesinde oluştururlar. Şu an için, beklametazon monohidrat, budesonid, flunisolid, triamsinolon asetonid, flutikazon (propiyonat ve furoat), mometazon furoat ve siklesonid piyasada bulunan nazal topikal kullanılabilen kortikosteroidlerdir. Bu preparatlar arasında klinik etkinlik açısından anlamlı farklılıklar yoktur.
Bu preparatlarla ilgili olarak lokal yanma ve batma hissi, irritasyon, kuruluk ve bazen burun kanaması topikal yan etkiler olarak karşımıza çıkabilmektedir.
Lökotrien antagositleri
Lökotrienler, mast hücreleri, eozinofiller, bazofiller ve makrofajlar tarafından üretilebilen araşidonik asitden sentezlenen inflamatuvar etkili lipid mediyatörlerdir. Nükleer membrandan posfolipaz A2 enzimi ile başlayan araşidonik asit ayrılma macerası lökotrien senteziyle devam eder. Araşidonik asit 5-lipooksijenaz (5-LO) enzimi aracılığı ile LTA4’ e metabolize olur. Ardından değişik konvertazlar aracılğı ile LTC4 LTD4 ve LTE4 oluşur. Bu lökotrienlere “sisteinil lökotrienler (CsyLTs)” diyoruz. CsyLTs’ in ciddi bronşiyal düz kas kasıcı, mukus üretimi artırıcı, ödem yapıcı ve vasküler permeabilite artırıcı etkileri vardır. LTD4, P-selektin yolağını güçlendirerek lökosit adezyonu ve lökositlerin inflamasyon alanına toplanmasını artırır. Ayrıca β2-integrinleri artırarak eozinofil adezyonunda da öenmli rol oynar. LD4 ile normal insanlarda yapılan nazal provokasyon sonucu, nazal mukozal kan akımının hızlandığı ve havayolu rezistansının arttığı gözlenmiştir.
Lökotrienler sentezleri ya da reseptörleri bloke edilerek fizyolojik olarak antagonize edilebilirler. Zileuton 5-LO sentez inhibitörü olup, alerjen provokasyonu sonrası AR’ li hastalarda ortaya çıkan nazal konjesyonu bloke edebilen farmakolojik bir üründür. Şu an için ise yalnızca Cys LT1 reseptör antagonisti olan montelukast AR için onay almış ve piyasada bulunan ürün olarak karşımıza çıkmaktadır. Montelukastın gün içerisinde ve gece yaşanan konjesyonu, burun akıntısını, burun kaşınması ve hapşırmayı, uykuya dalmadaki zorlanmayı, gece uykudan uymaları düzelttiği gözlenmektedir. Periferik eozinofil sayısını düşürdüğü ve anti-inflamatuvar etkiyi de bu sayede oluşturduğu düşünülmektedir. Ancak, tüm bunlara rağmen bu etkileri açısından intranazal kortikosteroidlerden çok daha az etkili olduğuna dair birçok yayın bulunmaktadır. Genel anlamda güvenilir bir preparat gibi görünmesine rağmen; ajitasyon agresyon, anksiyete, halüsinasyon, depresyon, insomni, irritabilite, huzursuluk ve intihar düşünceleri gibi bazı psikiyatrik yan etkilerinden bahsedilmektedir.
Nazal dekonjestanlar
Bu ilaçlar nazal kapasitans damar endotellerindeki α1 ve α2 adrenerjik reseptörleri antagonize ederek nazal kan akımını yavaşlatırlar. Bu sayede nazal mukozal konjesyon ve şişliği azaltırlar. Bir antihistaminikle kombine edildiklerinde daha iyi sonuçlar alınabilmektedir. Katekolaminlerden olan pseudoefedrin ve fenilefrin oral uygulanabilecek formlara sahiptir. Burun akması semptomları toparlayabilmesine rağmen, burundaki kaşıntı, hapşırma ve göz semptomları üzerine herhangi bir etkileri yoktur. İmidazolin deriveleri olan oksimetazolin, ksilometazolin ve nafazolin intranazal kullanım için uygundur. Hızlı intranazal dekonjestan olmaları ve daha az yan etkili olmalarına rağmen, ilaç bırakıldığında ciddi rebound konjensyon etkileri ortaya çıkar. Bazı yayınlarda oksimetazolin için T hücrelerini ve IL-1β, TNF-α, IL-6 ve IL-8 gibi sitokinleri inhibe ettiğinden bahsedilmektedir. Bu preparatlarla ilgili bazı lokal nazal yan etkiler dışında oral yoldan kullanıklarında sinirlilik, uykusuzluk, irritabilite, baş ağırısı, taşikardi, hipertansiyon, göz içi basınç artışı, idrar zorluğu gibi sistemik yan etkiler de tanımlanmıştır. Bu sebeple AR’ de bu ilaçların ya kısa süreli ya da aralıklı kullanılmaları tavsiye edilmektedir.
Mast hücre stabilizatörleri
Alerjenle tekrar karşılaşma sonucu mast hücrelerinin degranülasyonu ile birçok mediyatör salınmakta birçok sitokin üretilmektedir. Sonuç olarak inflamatuvar hücrelerin de olaya katıldığı bir alerjik inflamasyon süreci yaşanmaktadır. Dolayısıyla alerjik hastalıkların tedavilerindeki önemli hedeflerden biri de mast hücresinin stabilizasyonu olmalıdır. AR’ de intranazal olarak uygulanan kromolinlerin mast hücre klorit kanallarını etkileyerek, hücre içine ekstrasellüler kalsiyum girişini inhibe ettikleri ve mast hücreleri satbilize ettikleri gösterilmiştir. Dolayısıyla kromolinler AR’ de hem erken hem de geç faz reaksiyonları engeller. Ayrıca makrofaj, eozinofil, monosit ve trambositlerin migrasyon ve yaşam sürelerini inhibe ettikleri gösterilmiştir. Nazal yanma, batma, hapşırma gibi minör yan etkiler % 10 gibi bir hasta grubunda oluşabilmektedir. Dual etkili olan olopatadin en sık kullanılan topikal nazal preparat olarak karşımıza çıkmaktadır.
Topikal antikolinerjik ajanlar
Nazal bezlerin asetilkolin ile parasempatik uyarımı sonucunda vazodilatasyon ve sulu burun akıntısına neden olduğu bilinmektedir. Antikolinerjiklerin muskarinik reseptörleri bloke etmesi sonucunda mukus sekresyonunda azalma, sulu burun akıntısı, nazal konjesyon ve hapşırmada azalma olmaktadır. Ancak AR’ de bu ilaçlar yalnızca topikal kullanıma uygundur. İpratropiyum bunların prototipidir. Ağız ve boğazda kuruluk, gözde irritasyon, görmede bulanıklık, konjunktivit, ses kısıklığı, öksürük, tad duyusunda bozulma gibi minör yan etkiler bu ilaçları kulananların %2’ sinde görülebilmektedir.
Alerjen spesifik immünoterapi
İmmünoterapi (SIT), duyarlı antijene karşı desensitizasyon oluşturmaktadır. Alerjen spesifik IgG4/IgE oranında belirgin bir artış sağlamakta; bunun yanında IL-10 gibi düzenleyici sitokinleri indükleyerek Th2/Th1 imbalansı üzerinde etkili olur ve sonuçta alerjik inflamasyon bölgesine efektör hücre toplanmasını ve bunların aktivasyonlarını inhibe etmektedir. Şu an için rutinde iki model olarak uygulanmaktadır: subkütan (SCIT) ve sublingual (SLIT) uygulama. SLIT’ nin SLIT’ e göre sistemik yan etkilerinin daha az olduğu görülmektedir. Ancak semptom kontrolü açısından da asla SCIT kadar etkili olamadığını görmekteyiz. Bunun dışında en etkili SIT yöntemi; alerjeni direkt olarak intra-lenfatik enjekte etme şeklinde yapılan uygulamalardır. Alergoidler, rekombinan alerjenler, kimyasal olarak değiştirilen alerjenler ve ve T-hücre epitop peptidleri gibi immünoterapi ajanları ile ilgili pozitif sonuçlar rapor edilmektedir.
Monoklonal anti-IgE antikorlar
Omaluzimab, dolaşan IgE antikorlarının Ce3 bölgesi ile kompleks yaparak mast hücreleri, ve bazofil gibi hücrelerdeki yüksek afinitedeki reseptörlere bağlanmasını bloke eden humanize, rekombinan, mono-klonal bir antikordur. AR’ li hastalarda dolaşan IgE düzeylerinde belirgin azalma yaparak klinik olarak çok ciddi iyilik sağladığını gösteren çok miktarda yayın vardır. Bunun yanında hem kan hem de dokudaki mast hücreleri üzerindeki FcR1 ekspresyonlarını azaltır. Nazal semptomları düzelttiği gibi, yaşam kalitesi düzeyini de yükseltmektedir. İyi tolere deilebilien, çok düşük oranda anafilaksi riski olan bir antikordur (0,9/1000 uygulama). Omalizumab ile birlikte uygulanan SIT tedavisinin tek başına uygulamalarda daha etkili olduğunu gösteren çalışmalar vardır. En önemli handikapı şu an için pahalı bir tedavi modeli olmasıdır.
Kapsaisin tedavisi, tamamlayıcı ve alternatif tıp, cerrahi
Kapsaisin nazal C-liflerinde eksprese olan vanilloid resertörlere bağlanmaktadır. Cilde ya da intranazal olarak tekrarlayan uygulamaların periferal sinir uçlarında desensitizasyona yol açtığı görülmüştür. Nörotransmiterlerin önemli rol oynadığı vazomotor rinitte işe yaramaktadır. AR’ de de nazal konjesyon, burun akması, hapşırma gibi semptomları azalttığı gözlenmiştir. Ancak buna rağmen özellikle ev tozu akarı duyalı PAR hastalarında klinik olarak efektivitesinin olmadığını gösteren yayınlar da vardır.
Serum fizyolojik ile nazal yıkama ya da irrigasyon AR’ de tamamlayıcı bir tedavi modelidir. Bu tedavi şeklinde sinüsler ve farinksin alerjen ve mukus ile olan kontağının azaltılması sağlanmaktadır. Aynı zamanda burun içindeki ödem de azaltılmaktadır. Nazal serum fizyolojik uygulamasının AR’ li çocuklarda topikal kortikosteroid ihtiyacını azalttığı gösterilmiştir.
Çocuklarda mikroplarla karşılaşmanın Th1 tipindeki immün yanıt gelişimi yanında IL-10 ve TGF-β inhibitör sitokinlerin ekspresyonunu arttırdığı gösterilmiştir. Yararlı mikroorganizmaların toll-like resptörler aracılığı bunu yaptığına dair kanıtlar vardır. Özellikle bifidobakteri ve laktobasillerin bu tür etkileri vardır. Bu tür probiyatioklerin AR’ de etkili olabileceğini gösteren çalışmalar vardır.
Akapunkturun AR’ de etkili olduğuna dair yeterli ve bilimsel kanıt yoktur.
UV-A ve UV-B’ nin kullanıldığı, hastaların ilaç kullanamadığı ya da yeterli yanıt alamadığı birkaç küçük seride sınırlı fayda verdiği belirtilmektedir. AR ile ilgili sedece bir çalışmada infrared radyasyon tedavisi (FIR) denenmiştir. Fır uygulamasının, oratama yaydığı ısı nedeniyle termo-reseptörleri etkilediği ve mikrosirkülasyonu artırması yoluyla etkili olabileceği belirtilmiştir.
Tıbbi tedaviye yanıt vermeyen sinüzit, nazal polip, büyümüş türbinatlar veya varsa nazal septal deviyasyona cerrahi olarak müdahale etmek faydalı olabilmektedir.
Yeni Tedavi Modelleri
Glukokortikoid reseptör agonistleri
Topikal glukortikoidler AR’ de birinci basamak tedaviyi oluşturmaktadırlar. Lokal uygulandıkları için ciddi sistemik yan etki oluşturmazlar. Ancak buna rağmen nazl uygulanan glukortikoidleri dolaşımda saptamak mümkündür. Şu an için bu tür yan etki risklerini bertaraf etmek adına selektif glukokortikoid reseptör agonistleri geliştirilmektedir. Yapılan çalışmalarda da oldukça etkili oldukları gözlenmiştir. Bunun dışında “glukokortikoid prodrug”lar da geliştirilmeye çalışılmaktadır.
Sitokin sentez inhibitörleri
AR’ deki sitokinlerin inflamasyondaki yerleri ortaya çıktıktan sonra AR tedavisi için bir çok sitokin sentezi inhibitörü çalışmaları başlamıştır. Şu ana kadar TNF-α, IFN- ve IL-8 üretimini bloke ederek potansiyel olarak AR tedavisinde kullanılabilecek ürünler rapor edilmiştir.
Fosfodiesteraz 4 (PDE4) inhibitörleri
PDE4 siklik AMP metabolizmasının izoenzimidir. PDE4 inhibitörleri ile sağlanan siklik AMP artışı sonucunda inflamatuvar süreçte inhibisyon olduğu gözlenmiştir. Roflumilast AR’ de kullanılan bir PDE4 inhibitörüdür. Aynı şekilde OX-914 de AR’ de etkili olmaktadır.
Bardikinin B2 reseptör agonistleri
Kininler inflamayona dierk ya da indirek katılan vazoaktif mediyatörlerdir. Mast hücresi ürünleri, prostanoidler, taşikininler, sitokinler ve NO gibi mediyatörlerin stimüle ederek indirek etkilerini gösterirler. Direk etkilerini ise B1 ve B2 reseptörlerine bağlanarak gösterirler. B2 reseptörler, endotelde, sinir liflerinde, lökositlerde ve mast hücrelerinde gösterilmiştir. B1 reseptörler ise bir çok dokuda az da olsa bulunmaktadırlar. İnflamasyon ya da şok gibi stresli durumlarda sitokinler aracılğı ile ekspresyonları artırılmaktadır. Bradikinin reseptörleri ile ilişkili mekanizma daha çok geç faz alerjik inflamasyonda çalışmaktadır. Güçlü bir B2 reseptör antagonisti olan JSM-10292 şu an için AR ve astımda preklinik çalışmalarda kullanılmaktadır. Bir başka B2 reseptör antagositi olan FK3657’ nin hayvan modellerinde astımın geç faz inlamasyonunda etkili olduğu ancak erken fazla ilişkili bir etkisinin olmadığı gösterilmiştir. Diğer bir B2 reseptör antagositi olan icatibant’ ın mite alerjiklerde mite ile provokasyon ve non-atopiklerde PAF ile indüklenen nazal aşırı cevaplılığı inhibe ettiği gözlenmiştir.
Histamin H4 reseptör antagonistleri/H1 reseptör antagonistleri/Dual H1 ve H3 reseptör antagonistleri
Levosetirizin ve bilastine yeni H1 antagonistlerdir. Ancak bunlardan daha az sedasyon ve kardiyovasküler yan etkisi olan ve aynı zamanda antienflamtuvar etkinliği olan yeni H1 antihistaminikler geliştirilmeye çalışılmaktadır. SUN-1334His bu moleküllerden biridir.
H1/H3 dual etkili antihistaminik ajanların nazal konjesyonda daha etkili olduğunu gösteren yayınlar vardır. GSK-835726 ve GSK-1004723 dual etkili antihistaminikler olup, in-vitro ve in-vivo iyi yanıtlar alındığı rapor edilmiştir.
H4 reseptörler, daha çok hematopoetik hücrelerde bulunmaktadır. Histamin ile indüklenen eozinofil migrasyonu, adezyon molekülü ekspresyonu ve aktin hücre iskeleti yeniden düzenlenmesinin H4 reseptörler aracılığı ile olduğunu biliyoruz. Araştırma aşamasında olan UR-63325, H4 antihistaminiktir. Bu ilaçla ilgili iyi sonuçlar bildirilmektedir.
PGD2 reseptör antagonistleri
PGD2, mast hücrelerinin degranülasyonu sonucu ortama salınan önemli bir prostanoiddir. Anyı zamanda, alerjik inflamasyonun önemli hücreleri olan Th2 ve dendritik hücrelerden de üretilmektedir. Etkilerini DP1 ve CRTH2 (DP2) reseptörler üzerinden göstermektedir. CRTH2 reseptörü uyarımı sonucunda hücre migrasyon ve adezyonu artırılmaktadır. Yine DP1 reseptörü uyarımı sonucu IL-12 sentesinde inhibisyon olduğu ve Th0’ dan Th2’ ye doğru gibidişin hızlandığı bilinmektedir. Ayrıca CRTH2 reseptör uyarımı sonrası Th2 tipi sitokin ve IgE sentezi hızlanmakatadır. Oral yoldan kullanılabilen CRTH2 antagonisti olan AM-211 ve AM-461 şu an için araştırma safhasındadır.
MAP kinaz inhibitörleri
MAP kinaz enzimi IL-1β, TNF-α, IL-6 gibi proinflamatuvar sitokinlerin, COX-2 gibi enzimlerin üretimini sağlayan sistem içerisinde yer almaktadır. Bu enzim ayrıca, immün sistem hücrelerinin proliferasyon ve diferansiyasyonlarını da düzenlemektedir. AR’ de MAP kinaz enzim inhibitörleri ile ilgili çalışmalar vardır.
Nitrik oksit (NO) sentaz inhibitörleri
AR’ de NO seviyelerinde ciddi artışlar mevcuttur. NO glandüler sekresyon ve vazodilatasyona sebep olan bir mediyatördür. NO sentaz inhibitörlerinin antijen, histamin ya da bradikinin ile uyarılan nazal plazma ekstravazasyonunu bloke ettiği gösterilmiştir. Ancak tekrarlayan intra nazal NO sentaz inhibitörlerinin kullanımı sonucu aşırıcevaplılık oluştuğu görülmüştür.
Nötrofil elastaz inhibitörleri
Nötrofil elastaz enzimi serin proteazlardan kimotripsin süperailesi üyesidir. Monosit ve mast hücrelerinde de azurofil granüllerde bulunmaktadır. Bu enzim sekrete edildiğinde nötrofillerin inflamasyon alanına göçünü artırmakla birlikte epitelyal ve endotelyal hücrelerden IL-6, IL-8, TGF-β ve GM-CSF üretimini artırırken, IL-1, TNF-α ve IL-2 yıkılımını da artırmaktadır. Literatüre bakıldığında patentli nötrofil elastaz inhibitörleri görülmektedir.
Toll-like reseptör sinyalleri
İmmünostimülatör etkili DNA sekansları CpG (sitozin fosforotioat guanozin) motifleri içerir. Bu motifler antijene immün cevap esnasında güçlü bir Th1 immünolojik yanıta neden olurlar. Bu sebeple AR de dahil bazı Th2 tipi immünolojik cevabın olduğu hastalıkların tedavilerinden denenmişlerdir. CpG DNA bakterilerde oldukça bol bulunur ve özellikle de innate immünitede görevli hücreler yüzeyinde bulunan TLR9 reseptörüne önemli derecede özgüllük gösteririler. Dendritik hücrelerin TLR sinyali le aktive olması güçlü bir Th1 immün yanıtına sebep olur. Bu tip bir yanıt, Th2 tipindeki yanıtı baskılamak için kullanılabilecek iyi bir yoldur. CpG motifleri ayrıca Th2 tipindeki sitokin reseptörlerinin (örneğin IL-4R) ekspresyonunun inhibisyonunda da oldukça etkilidir. Hayvan modellerinde CpG DNA uygulamalarının nazal semptomları, eozinofilik inflamayonu ve hava yolu aşırı cevaplılığını azalttığı görterilmiştir. Alerjenle DNA konjugasyonu sonucu elde edilen praparatın uygulanması ile TLR7/8 resepötlerinin aktivasyona uğradığı, AR ve astımda iyi sonuçlar alındığı bildirilmektedir.
TSLP/OX40L inhibisyonu
Timik stromal lenfopoetin (TSLP) son dönemlerde alerjik inflamasyonda rolü olduğu kanıtlanan bir moleküldür. İnsanlarda AR ve benzeri alerjik hastalık durumlarında dokularda aberan TSLP ekspresyonları olduğu gözlenmiştir. TSLP genel olarak hasarlı epitelyal hücrelerce üretilmekte ve ortamda bulunan myeloid denditirk hücreleri aktive ederek naive CD4+ T lenfositlerin Th2 fenotitipine dönüşünü sağlamaktadır. TSLP ayrıca bir TNF süperailesi üyesi olan OX40L aracılığı ile CD4+Th2 hafıza hücre gelişmine ve IL-12 üretiminin önelnmesine neden olmaktadır. TSLP ile ilişkili Th2 tipindeki patogenik inflamasyonu değiştirmeye aday iki adjuvan tanımlanmıştır. Bunlardan bir BCG, diğeri ise imidazokinolindir. İmidazokinolin TLR7 ve TLR8 in özgül ligandı olarak görülmektedir. Her iki ajan dendritik hücre bağımlı Th hücre gelişiminde ciddi Th1 polarizasyonu sağlar. Aynı zamanda ikisi de dendritik hücrelerden OX40L ekspresyonunu güçlü bir şekilde inhibe ederler. Bu etkileri sayesinde her iki adjuvanın da alerjik inflamatuvar yanıtı bu iki yolakla inhibe etme olanakları vardır.
Peptid bazlı immünoterapi
T hücre epitoplarına tekabül eden, kısa, sentetik, alerjenden derive peptidlerin immünolojik toleransı indükleri gözlenmiştir. T hücre peptid epitopları ile yapılan aşılama çalışmaları sonucu mast hücresi ya da basofillerde IgE’ lerin çapraz bağlanmalarının inhibe edildiği, antijen spesifik Treg hücrelerinin indüklendiği ve IL-4 üretiminde azalma sağlandığı rapor edilmiştir. Alerjen immünoterapiye göre IgE bağımlı sistemik yan etkilerin de çok daha az rastlandığı ortaya konulmuştur.
Very late antijen-4 (α4β1 integrin) antagositleri
İntegrinler vasküler endotelyumdan lökosit geçişi için gerekli mediyatörler olarak bilinmektedirler. VLA-4 bir VCAM-1 reseptörü olarak eozinofiller, lenfositler ve monositlerde bulunmaktadır. VCAM-1, vasküler endotelde, hava yolu epitelinde fibroblastlarda ve hava yolu düz kas hücrelerinde yaygın olarak bulunmakta ve VLA- ile ilişkiye girip inflamatuvar hücrelerin inflamasyon alanına göçünü düzenlemektedir. Natalizumab VLA-4 inhibitörü olan bir monoklonal antikordur. Son dönemlerde koyun astım modelinde ağız yoluyla kullanılan VLA-4 antagonisleri rapor edilmektedir.
Triptaz inhibitörleri
Β-Triptaz mast hücre granüllerinde en bol bulunan nötral protez yapıda inflamatuvar bir mediyatördür. Şu an için triptaz inhibitörleri ile bazı çalışmalar yapılmaktadır. Aerosol fromunun uygulandığı hayvan modellerinde geç faz bronkokonstrüksiyonu engellediği gösterilmiştir. APC-366 isimli peptidic inhibitörün intradermal uygulanması sonucunda antijene verilen kütanöz cevabın bloke edildiği görülmüştür.
İyon kanal blokerleri
Mast hücrelerinde IgE bağımlı kalsiyumla aktive olan potasyum kanalları ve kalsiyumdan bağımsız klor kanalları bulunmaktadır. Bu kanalların blokajı sonucu mast hücrelerinin degranülasyona daha dayanıklı oldukları görülmüştür. Bu hedeflere yönelik yeni ilaç çalışmları sürmektedir.
Sonuç
AR ve n-AR heterojen patogenetik mekanizmalara sahip hastalıklardır. Bu nedenle tedavisinde kullanılanacak olan yöntemler de heterojenite göstermektedir. Şu an için küratif tedavi adayları olmakla birlikte konu ile ilgili olarak tüm hasta bireyler kendine özgü ele alınmalıdır. Klinik uygulama ve gözlemlerimiz gösteriyor ki bu tedaviler tek başına değil kombinasyonlar şeklinde uygulanırsa daha iyi sonuçlar alınmaktadır. Tedavideki temel amacımız patogenetik anormallikleri çözmek olsa da en az yan etkili, en ucuz ve yaşam kalitesini en iyi düzeye getiren akılcı ilaç seçimi halen bizler için bir zorunluluktur.
Kaynaklar
1- Kirmaz C, Ozenturk Kirgiz O, Bayrak P, et al. Effects of allergen-specific immunotherapy on functions of helper and regulatory T cells in patients with seasonal allergic rhinitis. Eur Cytokine Netw. 2011 Mar;22(1):15-23.
2- Rondón C, Fernandez J, Canto G, Blanca M. Local allergic rhinitis: concept, clinical manifestations, and diagnostic approach. J Investig Allergol Clin Immunol. 2010;20(5):364-71.
3- Kemp AS. Allergic rhinitis. Paediatr Respir Rev. 2009 Jun;10(2):63-8.
4- Vichyanond P. Omalizumab in allergic diseases, a recent review. Asian Pac J Allergy Immunol. 2011 Sep;29(3):209-19.
5- Sin B, Togias A. Pathophysiology of allergic and nonallergic rhinitis. Proc Am Thorac Soc. 2011 Mar;8(1):106-14.
6- Amin K. The role of mast cells in allergic inflammation. Respir Med. 2012 Jan;106(1):9-14.
7- Ito T, Liu YJ, Arima K. Cellular and molecular mechanisms of TSLP function in human allergic disorders–TSLPprograms the “Th2 code” in dendritic cells. Allergol Int. 2012 Mar;61(1):35-43.
8- Mandhane SN, Shah JH, Thennati R. Allergic rhinitis: an update on disease present treatments and future prospects. Int Immunopharmacol. 2011 Nov;11(11):1646-62.
Sağlıklı günler dileğiyle…
Prof. Dr. Cengiz KIRMAZ

